
세프리프 ®, 이온교환 크로마토그래피에 대해 알아야 할 모든 것
이온교환 크로마토그래피 소개:
이온교환 크로마토그래피는 이온교환기 상의 교환 가능한 이온과 주변 매질에서 분리된 다양한 이온 사이의 정전기력 차이를 이용하는 컬럼 크로마토그래피 방법으로, 교환 평형을 통해 분리의 목적을 달성합니다. 이온교환 크로마토그래피는 높은 감도, 반복성, 좋은 선택성, 빠른 분석 속도의 장점을 가지고 있으며, 현재 가장 일반적으로 사용되는 크로마토그래피 방법 중 하나입니다.
1848년 톰슨 등은 토양 내 알칼리성 물질의 교환을 연구하는 과정에서 이온교환 현상을 발견했다. 1940년대에는 안정된 교환 특성을 가진 폴리스티렌 이온교환 수지가 등장했다. 1950년대에는 이온교환 크로마토그래피가 생화학 분야에 진출하여 아미노산 분석에 응용되었다. 현재도 이온교환 크로마토그래피는 생화학 분야에서 여전히 널리 쓰이는 크로마토그래피 방법으로, 아미노산, 단백질, 당, 바이러스, 뉴클레오타이드 등 다양한 생화학 물질의 분리 정제에 널리 사용되고 있다.
이온 교환 과정:
이온 교환기와 용액 속의 이온 또는 이온 화합물 사이의 반응은 주로 이온 교환에 의해 수행됩니다. 수행되는 이온 교환 반응은 가역적입니다. RA가 양이온 교환기를 나타낸다고 가정하면, 용액에서 해리된 양이온 A+는 용액 속의 양이온 B+와 가역적 교환 반응을 겪을 수 있으며, 반응식은 다음과 같습니다.
RA + B + RB + A +
반응은 매우 빠른 속도로 평형에 도달하며, 평형 이동은 질량 작용의 법칙을 따릅니다.
이온 교환기의 선택성은 반응의 평형 상수 K로 표현할 수 있습니다.
K강초RB][A+]/[RA][B+]
✔반응 용액에서 [A+]가 [B+]와 같으면 K=[RB]/[RA]가 됩니다.
✔K>1, 즉 [RB]>[RA]이면 이온교환체의 B+에 대한 결합력이 A+에 대한 결합력보다 크다는 것을 의미한다.
✔K=1, 즉 [RB]=[RA]이면 이온교환체는 A+와 B+에 대하여 동일한 결합력을 갖는다는 것을 의미한다.
✔K
✔K 값은 이온교환체의 다양한 이온에 대한 결합력이나 선택성을 반영하는 매개변수이므로, K 값을 이온교환체의 A+와 B+에 대한 선택성 계수라고 합니다.
이온교환의 메커니즘:
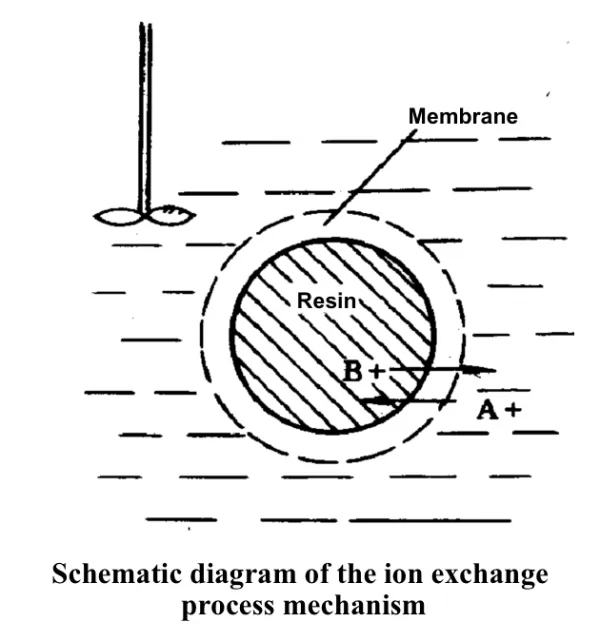
A+는 용액에서 수지 표면으로 확산됩니다.
A+는 수지 표면으로부터 수지 내부의 활성 중심으로 들어간다.
A+는 활성 중심의 RB와 복분해 반응을 겪습니다.
탈착된 이온 B+는 수지 내부에서 수지 표면으로 확산된다.
B+ 이온은 수지 표면에서 용액으로 확산됩니다.
환율을 제어하는 단계는 확산 속도인데, 이는 다양한 분리 시스템에서 내부 확산 또는 외부 확산을 통해 제어될 수 있습니다.
이온 교환 공정에 영향을 미치는 요인:
✔입자 크기: 작을수록 빠릅니다.
✔가교도 : 가교도 적고 교환속도 빠름
✔온도 : 높을수록 더 빨리 확산계수의 증가와 관련이 있습니다
✔이온 원자가: 원자가가 높을수록 확산 속도가 느려집니다.
✔이온 크기: 작을수록 빠릅니다.
✔ 교반속도 : 어느 정도 크면 빠를수록 좋다
✔용액 농도 : 교환율이 확산에 의해 조절되는 경우 농도가 클수록 교환율이 빨라집니다.
이온교환의 원리:
양이온 교환 수지를 선택하면 양전하 물질이 H+와 교환되어 수지에 결합됩니다. 음이온 교환 수지를 선택하면 음전하 물질이 OH-와 교환되어 수지에 결합될 수 있습니다.
수지 상에서 물질들의 결합의 단단함의 정도에는 차이가 있으며, 혼합물 속의 성분들은 적절한 용출액을 선택하여 하나하나 용출시켜 분리·정제의 목적을 달성할 수 있습니다.
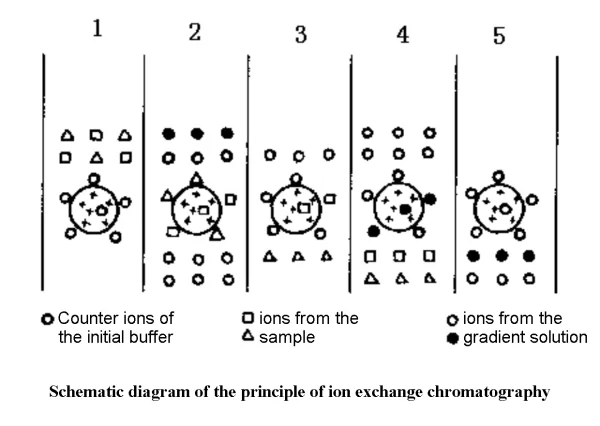
✔1. 평형단계 : 이온교환기와 상대이온의 결합
✔2. 흡착 단계 : 샘플 및 상대 이온 교환
✔3. 탈착 단계 : 그래디언트 완충 용액은 먼저 약하게 흡착된 물질을 씻어내고, 그 다음에 강하게 흡착된 물질을 씻어냅니다.
✔4. 재생 단계: 원래의 균형 솔루션으로 완전히 세척하여 재사용 가능
이온교환 크로마토그래피 수지:
양이온 교환체의 하전된 그룹은 음전하를 띠고, 반대 이온은 양전하를 띠는데, 이는 용액 내의 양이온이나 양전하 화합물과 교환 반응을 수행할 수 있습니다.
하전기의 세기에 따라 강산형(술폰산을 갖는 기, R-SO3H), 중강산형(인산기 또는 아인산기를 갖는 기, R-PO3H2), 약산형(카르복실기와 페놀계 수지, R-COOH 또는 R-벤젠고리-OH)의 세 가지 유형으로 나눌 수 있습니다.
이러한 교환체가 교환되는 동안 수소 이온은 다음 공식에 표시된 대로 이물질 양이온으로 대체됩니다.
R锛岰OOH锛婲a+锛漅锛岰OONa锛嬶紜H+
음이온교환기는 매트릭스에 4차아민[-N(CH3)3], 3차아민[-N(CH3)2], 2차아민[-NHCH3] 및 1차아민[-NH2] 그룹을 도입하여 형성된다.
아민기의 알칼리도 수준에 따라 세 가지 유형으로 나눌 수 있다. 각각 강염기성(4차 아미노기 포함), 약염기성(3차, 2차 아미노기 포함), 중염기성(강염기성과 약염기성기 모두 포함)이다.
이들이 용액 속의 이온과 교환될 때 반응식은 다음과 같습니다.
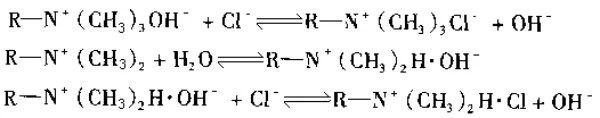
이온교환 크로마토그래피 수지의 특정 유형에 대한 자세한 내용은 이온교환 크로마토그래피에 관한 다음 기사를 참고하시기 바랍니다.















